中國藥典2020版穩(wěn)定性試驗指導原則征求意見稿 9001 原料藥物與制劑穩(wěn)定性試驗指導原則 (標注紅色表示將刪除,標注藍色表示新增) 一、原料藥物 原料藥物要進行以下試驗。 (一)影響因素試驗 此項試驗是在比加速試驗更激烈的條件下進行。其目的是探討藥物的固有穩(wěn)定性、了解影響其穩(wěn)定性的因素及可能的降解途徑與降解產(chǎn)物,為制劑生產(chǎn)工藝、包裝、貯存條件和建立降解產(chǎn)物分析方法提供科學依據(jù)。供試品可以用1批原料藥物進行,將供試品置適宜的開口容器中(如稱量瓶或培養(yǎng)皿),攤成≤5mm 厚的薄層,疏松原料藥物攤成≤10mm 厚的薄層,進行以下試驗。當試驗結(jié)果發(fā)現(xiàn)降解產(chǎn)物有明顯的變化,應考慮其潛在的危害性,必要時應對降解產(chǎn)物進行定性或定量分析。 (1)高溫試驗試品開口置適宜的潔凈容器中,60℃溫度下放置 10 天,于第 5天和第 10 天取樣,按穩(wěn)定性重點考察項目進行檢測。若供試品含量低于規(guī)定限度,則在 40℃條件下同法進行試驗。若 60℃:無明顯變化,不再進行 40℃試驗。 (2)高濕試驗供試品開口置恒濕密閉容器中,在 25℃分別于相對濕度 90%±5% 條件下放置 10 天,于第 5 天和第 10 天取樣,按穩(wěn)定性重點考察項目要求檢測,同時準確稱量試驗前后供試品的重量,以考察供試品的吸濕潮解性能。若吸濕增重5% 以上,則在相對濕度 75%±5%條件下,同法進行試驗;若吸濕增重 5% 以下,其他考察項目符合要求,則不再進行此項試驗。恒濕條件可在密閉容器如干燥器下部放置飽和鹽溶液,根據(jù)不同相對濕度的要求,可以選擇 NaCl 飽和溶液(相對濕度 75%±1%,15.5?60℃),KNO3 飽和溶液(相對濕度 92.5%, 25℃) 。 (3)強光照射試驗供試品開口放在裝有日光燈的光照箱或其他適宜的光照裝置內(nèi),光源可選擇任何輸出相似于 D65/ID65 發(fā)射標準的光源,或同時暴露于冷白熒光燈和近紫外燈下,并于照度為 4500Lx± 500Lx 的條件下放置 10 天,于第 5 天和第 10 天取樣,按穩(wěn)定性重點考察項目進行檢測,特別要注意供試品的外觀變化。 關(guān)于光照裝置,建議采用定型設(shè)備“可調(diào)光照箱”,也可用光櫥,在箱中安裝日光燈數(shù)相應光源使達到規(guī)定照度。箱中供試品臺高度可以調(diào)節(jié),箱上方安裝抽風機以排除可能產(chǎn)生的熱量,箱上配有照度計,可隨時監(jiān)測箱內(nèi)照度,光照箱應不受自然光的干擾,并保持照度恒定,同時防止塵埃進人光照箱內(nèi)。 此外,根據(jù)藥物的性質(zhì)必要時可設(shè)計試驗:原料藥在溶液或混懸液狀態(tài)時,或在較寬 pH 值范圍探討 pH 值與氧及其他條件應考察對藥物穩(wěn)定性的影響,并研究分解產(chǎn)物的分析方法。創(chuàng)新藥物應對分解產(chǎn)物的性質(zhì)進行必要的分析。冷凍保存的原料藥物,應驗證其在多次反復凍融條件下產(chǎn)品質(zhì)量的變化情況。在加速或長期放置條件下已證明某些降解產(chǎn)物并不形成,則可不必再做專門檢查。 (二)加速試驗 此項試驗是在加速條件下進行。其目的是通過加速藥物的化學或物理變化,探討藥物的穩(wěn)定性,為制劑設(shè)計、包裝、運輸、貯存提供必要的資料。供試品要求 3 批,按市售包裝,在溫度 40℃±2℃、相對濕度 75%±5%的條件下放置 6 個月。所用設(shè)備應能控制溫度±2℃、相對濕度±5% ,并能對真實溫度與濕度進行監(jiān)測。在試驗期間第 1 個月、2 個月、3 個月、6 個月末分別取樣一次,按穩(wěn)定性重點考察項目檢測。在上述條件下,如 6 個月內(nèi)供試品經(jīng)檢測不符合制訂的質(zhì)量標準,則應在中間條件下即在溫度 30℃± 2℃、相對濕度 65%±5% 的情況下(可用 Na2CrO4 飽和溶液,30℃,相對濕度 64.8%)進行加速試驗,時間至少 12 個月,應包括所有的考察項目,檢測至少包含初始和末次的4個時間點(如 0、6、9、12 月)。加速試驗,建議采用隔水式電熱恒溫培養(yǎng)箱(20?60℃)。箱內(nèi)放置具有一定相對濕度飽和鹽溶液的干燥器,設(shè)備應能控制所需溫度,且設(shè)備內(nèi)各部分溫度應該均勻,并適合長期使用。也可采用恒濕恒溫箱或其他適宜設(shè)備。 對溫度特別敏感的藥物,預計只能在冰箱中(4?8℃)保存,此種藥物的加速試驗,可在溫度 25℃±2℃、相對濕度 60%±10%的條件下進行,時間為 6 個月。 對擬冷凍貯藏的藥物,應對一批樣品在溫度(如:5℃±3℃或 25℃±2℃)下放置適當?shù)臅r間進行試驗,以了解短期偏離標簽貯藏條件(如運輸或搬運時)對藥物的影響。 (三)長期試驗 長期試驗是在接近藥物的實際貯存條件下進行,其目的是為制定藥物的有效期提供依據(jù)。供試品 3 批,市售包裝,在溫度 25℃±2℃,相對濕度 60%± 10%的條件下放置 12 個月,或在溫度 30℃±2℃、相對濕度 65%±5% 的條件下放置 12 個月,這是從我國南方與北方氣候的差異考慮的,至于上述兩種條件選擇哪一種由研究者確定。每 3 個月取樣一次,分別于 0 個月、3 個月、6 個月、9 個月、12 個月取樣按穩(wěn)定性重點考察項目進行檢測。12 個月以后,仍需繼續(xù)考察,分別于 18 個月、24 個月、36 個月,取樣進行檢測。將結(jié)果與 0 個月比較,以確定藥物的有效期。由于實驗數(shù)據(jù)的分散性,一般應按 95%可信限進行統(tǒng)計分析,得出合理的有效期。如 3 批統(tǒng)計分析結(jié)果差別較小,則取其平均值為有效期,若差別較大則取其短的為有效期。如果數(shù)據(jù)表明,測定結(jié)果變化很小,說明藥物是很穩(wěn)定的,則不作統(tǒng)計分析。 對溫度特別敏感的藥物,長期試驗可在溫度 6℃± 2℃的條件下放置 12 個月,按上述時間要求進行檢測,12 個月以后,仍需按規(guī)定繼續(xù)考察,制訂在低溫貯存條件下的有效期。 對擬冷凍貯藏的藥物,長期試驗可在溫度-20℃±5℃的條件下至少放置 12個月。 長期試驗采用的溫度為 25℃±2℃、相對濕度為 60%±10%,或溫度 30℃±2℃、相對濕度 65%±5%,是根據(jù)氣候帶制定的。氣候帶見下表。 二、藥物制劑 藥物制劑穩(wěn)定性研究,首先應查閱原料藥物穩(wěn)定性有關(guān)資料,特別了解溫度、濕度、光線對原料藥物穩(wěn)定性的影響,并在處方篩選與工藝設(shè)計過程中,根據(jù)主藥與輔料性質(zhì),參考原料藥物的試驗方法,進行影響因素試驗、加速試驗與長期試驗, 符合一定條件可以應用括號法和矩陣法簡化試驗方案。 (一)影響因素試驗 藥物制劑進行此項試驗的目的是考察制劑處方的合理性與生產(chǎn)工藝及包裝條件。供試品用 1 批進行,將供試品如片劑、膠囊劑、注射劑(注射用無菌粉末如為西林瓶裝,不能打開瓶蓋,以保持嚴封的完整性),除去外包裝,置適宜的開口容器中,進行髙溫試驗、高濕度試驗與強光照射試驗,試驗條件、方法、取樣時間與原料藥相同,重點考察項目見附表。 對于需冷凍保存的中間產(chǎn)物或藥物制劑,應驗證其在多次反復凍融條件下產(chǎn)品質(zhì)量的變化情況。 (二)加速試驗 此項試驗是在加速條件下進行,其目的是通過加速藥物制劑的化學或物理變化,探討藥物制劑的穩(wěn)定性,為處方設(shè)計、工藝改進、質(zhì)量研究、包裝改進、運輸、貯存提供必要的資料。供試品要求 3 批,按市售包裝,在溫度 40℃±2℃、相對濕度 75%±5% 的條件下放置 6 個月。所用設(shè)備應能控制溫度±2℃、相對濕度±5%,并能對真實溫度與濕度進行監(jiān)測。在試驗期間第 1 個月、2 個月、3個月、6 個月末分別取樣一次,按穩(wěn)定性重點考察項目檢測。在上述條件下,如 6 個月內(nèi)供試品經(jīng)檢測不符合制訂的質(zhì)量標準,則應在中間條件下即在溫度 30℃ ±2℃、相對濕度 65%±5%的情況下進行加速試驗,時間至少 12 個月,應包括所有的考察項目,檢測至少包含初始和末次的 4 個時間點(如 0、6、9、12 月)。 溶液劑、混懸劑、乳劑、注射液等含有水性介質(zhì)的制劑可不要求相對濕度。試驗所用設(shè)備與原料藥物相同。 對溫度特別敏感的藥物制劑,預計只能在冰箱(4?8℃)內(nèi)保存使用,此類藥物制劑的加速試驗,可在溫度 25℃±2℃,相對濕度 60% ±10%的條件下進行,時間為 6 個月。 對擬冷凍貯藏的制劑,應對一批樣品在溫度(如:5℃±3℃或 25℃±2℃)下放置適當?shù)臅r間進行試驗,以了解短期偏離標簽貯藏條件(如運輸或搬運時)對制劑的影響。 乳劑、混懸劑、軟膏劑、乳膏劑、糊劑、凝膠劑、眼膏劑、栓劑、氣霧劑、泡騰片及泡騰顆粒宜直接采用溫度 30℃±2℃、相對濕度 65%±5%的條件進行試驗,其他要求與上述相同。 對于包裝在半透性容器中的藥物制劑,例如低密度聚乙烯制備的輸液袋、塑料安瓿、眼用制劑容器等,則應在溫度 40℃±2℃、相對濕度 25%±5%的條件(可用 CH3COOK•1.5 H2O 飽和溶液)進行試驗。 (三)長期試驗 長期試驗是在接近藥品的實際貯存條件下進行,其目的是為制訂藥品的有效期提供依據(jù)。供試品 3 批,市售包裝,在溫度 25℃±2℃、相對濕度 60%±10%的條件下放置 12 個月,或在溫度 30℃±2℃、相對濕度 65%±5% 的條件下放置 12 個月,這是從我國南方與北方氣候的差異考慮的,至于上述兩種條件選擇哪一種由研究者確定。每 3 個月取樣一次,分別于 0 個月、3 個月、6 個月、9個月、12 個月取樣,按穩(wěn)定性重點考察項目進行檢測。12 個月以后,仍需繼續(xù)考察,分別于 18 個月、24 個月、36 個月取樣進行檢測。將結(jié)果與 0 個月比較以確定藥品的有效期。由于實測數(shù)據(jù)的分散性,一般應按 95%可信限進行統(tǒng)計分析,得出合理的有效期。如 3 批統(tǒng)計分析結(jié)果差別較小,則取其平均值為有效期限。 若差別較大,則取其短的為有效期。數(shù)據(jù)表明很穩(wěn)定的藥品,不作統(tǒng)計分析。 對溫度特別敏感的藥品,長期試驗可在溫度 6℃±2℃的條件下放置 12 個月,按上述時間要求進行檢測,12 個月以后,仍需按規(guī)定繼續(xù)考察,制訂在低溫貯存條件下的有效期。 對擬冷凍貯藏的制劑,長期試驗可在溫度-20℃±5℃的條件下至少放置 12 個月,貨架期應根據(jù)長期試驗放置條件下實際時間的數(shù)據(jù)而定。 對于包裝在半透性容器中的藥物制劑,則應在溫度 25℃±2℃、相對濕度 40%±5%,或 30℃±2℃、相對濕度 35%±5%的條件進行試驗,至于上述兩種條件選擇哪一種由研究者確定。 對于生物制品,應充分考慮運輸路線、交通工具、距離、時間、條件(溫度、濕度、振動情況等)、產(chǎn)品包裝(外包裝、內(nèi)包裝等)、產(chǎn)品放置和溫度監(jiān)控情況(監(jiān)控器的數(shù)量、位置等)等對產(chǎn)品質(zhì)量的影響。 此外,有些藥物制劑還應考察臨用時配制和使用過程中的穩(wěn)定性。例如,應對配制或稀釋后使用、在特殊環(huán)境(如高原低壓、海洋高鹽霧等環(huán)境)使用的制劑開展相應的穩(wěn)定性研究,同時還應對藥物的配伍穩(wěn)定性進行研究,為說明書/標簽上的配制、貯藏條件和配制或稀釋后的使用期限提供依據(jù)。 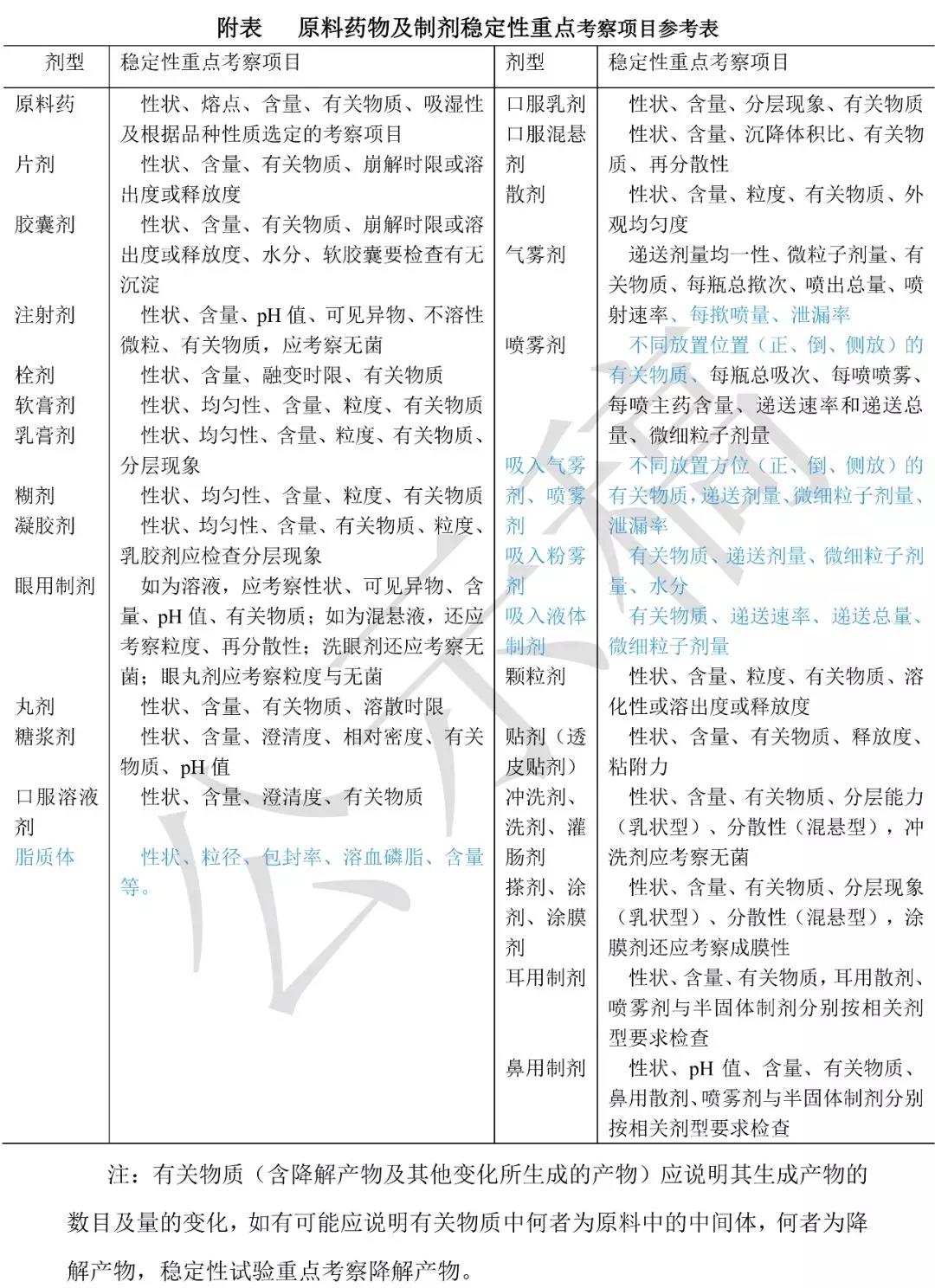
|